Учебник по Физике.
Оглавление учебника
Основные положения молекулярно-кинетической теории (МКТ).
Фундаментом молекулярно-кинетической теории является гипотеза, что все тела в природе состоят из мельчайших структурных единиц - атомов и молекул (комбинаций атомов). Атомистическая гипотеза зародилась 2500 лет назад в Древней Греции (Левкипп и Демокрит из Абдеры) и была окончательно сформулирована в трудах европейских ученых XIX в. За сто лет до этого выдающийся русский ученый-энциклопедист М. В. Ломоносов рассматривал тепловые явления как результат движения частиц, образующих тела.Основные положения.
Вещество состоит из атомов (молекул). Размеры атомов (молекул) равны 10-10 - 10-9 м. Число атомов (молекул) в единице объема вещества (твердого тела или жидкости) порядка 1022 частиц в 1 см3.
Атомы (молекулы) вещества находятся в непрерывном хаотическом тепловом движении. Наиболее яркое доказательство - броуновское движение (Р. Броун, 1827 г.) мелких частиц, взвешенных в жидкости, происходящее из-за непрерывных беспорядочных соударений этих частиц с молекулами жидкости. Другой простой экспериментальный факт, доказывающий тепловое движение атомов вещества, это диффузия.
Между атомами (молекулами) вещества действуют силы притяжения и отталкивания, зависящие от расстояния между частицами. На далеких расстояниях (превышающих несколько радиусов молекулы) взаимодействие слабо и носит характер притяжения, быстро убывающего с ростом расстояния (сила притяжения меняется как r-7). Физически это слабое притяжение обусловлено наличием электрического дипольного момента у электронейтральной в целом молекулы. С уменьшением расстояния это притяжение сначала несколько возрастает, а затем стремится к нулю. В момент соприкосновения электронных оболочек молекул возникают быстро растущие с уменьшением расстояния силы электростатического отталкивания.
Характер теплового движения молекул зависит от того, в каком агрегатном состоянии (твердом, жидком или газообразном) находится вещество. Расстояние между отдельными молекулами (атомами) в газах очень велико по сравнению с размерами самих молекул. Поэтому силы притяжения между молекулами в газе пренебрежимо малы. Следовательно, газы могут неограниченно расширяться, занимая любой предоставленный им объем. Молекулы в жидкости расположены достаточно близко друг к другу, так что при попытке сжатия жидкости возникают большие силы отталкивания. Отсюда малая сжимаемость жидкостей. С другой стороны, всякая внешняя сила заставляет молекулы жидкости перемещаться, что объясняет текучесть жидкости. В твердом теле атомы или молекулы могут лишь колебаться вокруг определенных положений равновесия. Поэтому твердые тела сохраняют и форму, и объем. У кристаллических твердых тел центры атомов (молекул) образуют пространственную решетку, в узлах которой находятся атомы вещества. Аморфные твердые тела не обладают жесткой структурой и скорее напоминают застывшие жидкости (в частности, под действием определенной силы аморфное тело может течь как жидкость).
Характеристики числа и массы атомов (молекул). Массы атомов (молекул) весьма малы в привычных единицах (порядка 10-26 кг), поэтому для их описания используют относительные единицы. По определению массу молекулы (атома) любого вещества m0 относят к 1/12 массы атома углерода m0C и называют относительной атомной массой Mотн:
 (1.1)
(1.1)Далее вводят понятие количества вещества. Если измерять его числом атомов (молекул), то получающиеся цифры настолько велики, что ими неудобно оперировать. Поэтому вводят единицу количества вещества - моль. По определению один моль равен количеству вещества, в котором содержится столько же атомов, сколько их содержится в 0,012 кг чистого углерода. Таким образом, число атомов в одном моле всех веществ одинаково. Оно называется числом Авогадро:
Количество вещества равно отношению числа атомов (молекул) этого вещества к числу Авогадро:
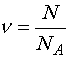 (1.2)
(1.2)Размерность: [n] = моль.
Молярная масса M равна массе вещества, взятого в количестве одного моля.
[M] = кг/моль. Из предыдущих определений следует, что молярная масса углерода равна ровно 0,012 кг. Молярная масса равна
где m0 - масса отдельного атома (молекулы). Масса m любого количества вещества, содержащего N атомов (молекул), равна
 (1.4)
(1.4)откуда количество вещества (в молях) равно
 (1.5)
(1.5)